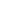النبات

مواضيع عامة في علم النبات

الجذور - السيقان - الأوراق

النباتات الوعائية واللاوعائية

البذور (مغطاة البذور - عاريات البذور)

الطحالب

النباتات الطبية


الحيوان

مواضيع عامة في علم الحيوان

علم التشريح

التنوع الإحيائي

البايلوجيا الخلوية


الأحياء المجهرية

البكتيريا

الفطريات

الطفيليات

الفايروسات


علم الأمراض

الاورام

الامراض الوراثية

الامراض المناعية

الامراض المدارية

اضطرابات الدورة الدموية

مواضيع عامة في علم الامراض

الحشرات


التقانة الإحيائية

مواضيع عامة في التقانة الإحيائية


التقنية الحيوية المكروبية

التقنية الحيوية والميكروبات

الفعاليات الحيوية

وراثة الاحياء المجهرية

تصنيف الاحياء المجهرية

الاحياء المجهرية في الطبيعة

أيض الاجهاد

التقنية الحيوية والبيئة

التقنية الحيوية والطب

التقنية الحيوية والزراعة

التقنية الحيوية والصناعة

التقنية الحيوية والطاقة

البحار والطحالب الصغيرة

عزل البروتين

هندسة الجينات


التقنية الحياتية النانوية

مفاهيم التقنية الحيوية النانوية

التراكيب النانوية والمجاهر المستخدمة في رؤيتها

تصنيع وتخليق المواد النانوية

تطبيقات التقنية النانوية والحيوية النانوية

الرقائق والمتحسسات الحيوية

المصفوفات المجهرية وحاسوب الدنا

اللقاحات

البيئة والتلوث


علم الأجنة

اعضاء التكاثر وتشكل الاعراس

الاخصاب

التشطر

العصيبة وتشكل الجسيدات

تشكل اللواحق الجنينية

تكون المعيدة وظهور الطبقات الجنينية

مقدمة لعلم الاجنة


الأحياء الجزيئي

مواضيع عامة في الاحياء الجزيئي


علم وظائف الأعضاء


الغدد

مواضيع عامة في الغدد

الغدد الصم و هرموناتها

الجسم تحت السريري

الغدة النخامية

الغدة الكظرية

الغدة التناسلية

الغدة الدرقية والجار الدرقية

الغدة البنكرياسية

الغدة الصنوبرية

مواضيع عامة في علم وظائف الاعضاء

الخلية الحيوانية

الجهاز العصبي

أعضاء الحس

الجهاز العضلي

السوائل الجسمية

الجهاز الدوري والليمف

الجهاز التنفسي

الجهاز الهضمي

الجهاز البولي


المضادات الحيوية

مواضيع عامة في المضادات الحيوية

مضادات البكتيريا

مضادات الفطريات

مضادات الطفيليات

مضادات الفايروسات

علم الخلية

الوراثة

الأحياء العامة

المناعة

التحليلات المرضية

الكيمياء الحيوية

مواضيع متنوعة أخرى

الانزيمات
ATP & Ubiquitin-Dependent Degradation
المؤلف:
Peter J. Kennelly, Kathleen M. Botham, Owen P. McGuinness, Victor W. Rodwell, P. Anthony Weil
المصدر:
Harpers Illustrated Biochemistry
الجزء والصفحة:
32nd edition.p280-281
2025-08-11
25
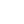
Degradation of regulatory proteins with short half-lives and of abnormal or misfolded proteins occurs in the cytosol, and requires ATP and ubiquitin. Named based on its presence in all eukaryotic cells, ubiquitin is a small (8.5 kDa, 76 residue) polypeptide that targets many intracellular proteins for degradation. The primary structure of ubiquitin is highly conserved. Only 3 of 76 residues differ between yeast and human ubiquitin. Figure 1 illustrates the three-dimensional structure of ubiquitin. Ubiquitin molecules are attached by non–α-peptide bonds formed between the carboxyl terminal of ubiquitin and the ε-amino groups of lysyl residues in the target protein (Figure 2). The residue present at its amino terminus affects whether a protein is ubiquitinated. Amino terminal Met or Ser residues retard, whereas Asp or Arg favor ubiquitination. Attachment of a single ubiquitin molecule to transmembrane proteins alters their subcellular localization and targets them for degradation. Soluble proteins undergo polyubiquitination, the ligase-catalyzed attachment of four or more additional ubiquitin molecules (Figure 1). Subsequent degradation of ubiquitin-tagged proteins takes place in the proteasome, a macromolecule that also is ubiquitous in eukaryotic cells. The proteasome consists of a macromolecular, cylindrical complex of proteins, whose stacked rings form a central pore that harbors the active sites of proteolytic enzymes. For degradation, a protein thus must first enter the central pore. Entry into the core is regulated by the two outer rings that recognize polyubiquitinated proteins (Figures 3 and 4).
Fig1. Three-dimensional structure of ubiquitin. Shown are α-helices (blue), β-strands (green), and the R-groups of lysyl residues (orange). Lys48 & Lys63 are sites for attachment of additional ubiquitin molecules during polyubiquitination. (Rogerdodd/Wikipedia)
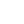
Fig2. Reactions involved in the attachment of ubiquitin (Ub) to proteins. Three enzymes are involved. E1 is an activating enzyme, E2 a transferase, and E3 a ligase. While depicted as single entities, there are several types of E1, and over 500 types of E2. The terminal COOH of ubiquitin first forms a thioester. The coupled hydrolysis of PPi by pyrophosphatase ensures that the reaction will proceed readily. A thioester exchange reaction now transfers activated ubiquitin to E2. E3 then catalyzes the transfer of ubiquitin to the ε-amino group of a lysyl residue of the target protein. Additional rounds of ubiquitination result in subsequent polyubiquitination.
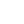
Fig3. Representation of the structure of a protea some. The upper ring is gated to permit only polyubiquitinated proteins to enter the proteosome, where immobilized internal proteases degrade them to peptides.
Fig4. An end-on view of a proteasome. (Thomas Splettstoesser/Wikipedia)
For the discovery of ubiquitin-mediated protein degradation, Aaron Ciechanover and Avram Hershko of Israel and Irwin Rose of the United States were awarded the 2004 Nobel Prize in Chemistry. Genetic disorders that result from defects in the genes that encode ubiquitin, ubiquitin ligases, or deubiquitinating enzymes include Angelman syndrome, autosomal recessive juvenile Parkinson disease, von Hippel-Lindau syndrome, and congenital polycythemia. For additional aspects of protein degradation and of ubiquitination, including its role in the cell cycle, see Chapters 4 and 35.
 الاكثر قراءة في الكيمياء الحيوية
الاكثر قراءة في الكيمياء الحيوية
 اخر الاخبار
اخر الاخبار
اخبار العتبة العباسية المقدسة

الآخبار الصحية















 "المهمة".. إصدار قصصي يوثّق القصص الفائزة في مسابقة فتوى الدفاع المقدسة للقصة القصيرة
"المهمة".. إصدار قصصي يوثّق القصص الفائزة في مسابقة فتوى الدفاع المقدسة للقصة القصيرة (نوافذ).. إصدار أدبي يوثق القصص الفائزة في مسابقة الإمام العسكري (عليه السلام)
(نوافذ).. إصدار أدبي يوثق القصص الفائزة في مسابقة الإمام العسكري (عليه السلام) قسم الشؤون الفكرية يصدر مجموعة قصصية بعنوان (قلوب بلا مأوى)
قسم الشؤون الفكرية يصدر مجموعة قصصية بعنوان (قلوب بلا مأوى)