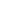النبات

مواضيع عامة في علم النبات

الجذور - السيقان - الأوراق

النباتات الوعائية واللاوعائية

البذور (مغطاة البذور - عاريات البذور)

الطحالب

النباتات الطبية


الحيوان

مواضيع عامة في علم الحيوان

علم التشريح

التنوع الإحيائي

البايلوجيا الخلوية


الأحياء المجهرية

البكتيريا

الفطريات

الطفيليات

الفايروسات


علم الأمراض

الاورام

الامراض الوراثية

الامراض المناعية

الامراض المدارية

اضطرابات الدورة الدموية

مواضيع عامة في علم الامراض

الحشرات


التقانة الإحيائية

مواضيع عامة في التقانة الإحيائية


التقنية الحيوية المكروبية

التقنية الحيوية والميكروبات

الفعاليات الحيوية

وراثة الاحياء المجهرية

تصنيف الاحياء المجهرية

الاحياء المجهرية في الطبيعة

أيض الاجهاد

التقنية الحيوية والبيئة

التقنية الحيوية والطب

التقنية الحيوية والزراعة

التقنية الحيوية والصناعة

التقنية الحيوية والطاقة

البحار والطحالب الصغيرة

عزل البروتين

هندسة الجينات


التقنية الحياتية النانوية

مفاهيم التقنية الحيوية النانوية

التراكيب النانوية والمجاهر المستخدمة في رؤيتها

تصنيع وتخليق المواد النانوية

تطبيقات التقنية النانوية والحيوية النانوية

الرقائق والمتحسسات الحيوية

المصفوفات المجهرية وحاسوب الدنا

اللقاحات

البيئة والتلوث


علم الأجنة

اعضاء التكاثر وتشكل الاعراس

الاخصاب

التشطر

العصيبة وتشكل الجسيدات

تشكل اللواحق الجنينية

تكون المعيدة وظهور الطبقات الجنينية

مقدمة لعلم الاجنة


الأحياء الجزيئي

مواضيع عامة في الاحياء الجزيئي


علم وظائف الأعضاء


الغدد

مواضيع عامة في الغدد

الغدد الصم و هرموناتها

الجسم تحت السريري

الغدة النخامية

الغدة الكظرية

الغدة التناسلية

الغدة الدرقية والجار الدرقية

الغدة البنكرياسية

الغدة الصنوبرية

مواضيع عامة في علم وظائف الاعضاء

الخلية الحيوانية

الجهاز العصبي

أعضاء الحس

الجهاز العضلي

السوائل الجسمية

الجهاز الدوري والليمف

الجهاز التنفسي

الجهاز الهضمي

الجهاز البولي


المضادات الحيوية

مواضيع عامة في المضادات الحيوية

مضادات البكتيريا

مضادات الفطريات

مضادات الطفيليات

مضادات الفايروسات

علم الخلية

الوراثة

الأحياء العامة

المناعة

التحليلات المرضية

الكيمياء الحيوية

مواضيع متنوعة أخرى

الانزيمات
General Reactions of Amino Acids
المؤلف:
D.M. Vasudevan, Sreekumari S., Kannan Vaidyanathan
المصدر:
Textbook of Biochemistry For Medical Students
الجزء والصفحة:
10th E ,P 24-25
2025-07-22
322
A. Due to Carboxyl Group
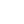
1. Decarboxylation: The amino acids will undergo alpha decarboxylation to form the corresponding amine (Fig.1). Thus some important amines are produced from amino acids. For example,
Histidine → Histamine + CO2
Tyrosine → Tyramine + CO2
Tryptophan → Tryptamine + CO2
Lysine → Cadaverine + CO2
Glutamic acid → Gamma amino butyric acid (GABA) + CO2
Fig1. Decarboxylation of amino acid
2. Amide Formation: The -COOH group of dicarboxylic amino acids (other than alpha carboxyl) can combine with ammonia to form the corresponding amide. For example,
Aspartic acid + NH3 → Asparagine
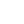
Glutamic acid + NH3 → Glutamine (Fig.2)
Fig2. Formation of glutamine
These amides are also components of protein structure. The amide group of glutamine serves as the source of nitrogen for nucleic acid synthesis.
B. Reactions Due to Amino Group
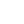
3. Transamination: The alpha amino group of amino acid can be transferred to alpha keto acid to form the corresponding new amino acid and alpha keto acid (Fig. 3). This is an important reaction in the body for the inter-conversion of amino acids and for synthesis of non-essential amino acids.
Fig3. Transamination reaction
4. Oxidative Deamination: The alpha amino group is removed from the amino acid to form the corresponding keto acid and ammonia.
In the body, Glutamic acid is the most common amino acid to undergo oxidative deamination.
5. Formation of carbamino compound: Carbon dioxide adds to the alpha amino group of amino acids to form carbamino compounds. The reaction occurs at alkaline pH and serves as a mechanism for the transport of carbon dioxide from tissues to the lungs by hemoglobin.
Hb—NH2 + CO2 → Hb—NH—COOH (Carbamino-Hb)
C. Reactions Due to Side Chains
6. Transmethylation: The methyl group of Methionine, after activation, may be transferred to an acceptor which becomes methylated.
Methionine + Acceptor → Methylated Acceptor + Homocysteine
7. Ester formation by the OH group: The hydroxy amino acids can form esters with phosphoric acid. In this manner the Serine and Threonine residues of proteins are involved in the formation of phosphoproteins. Similarly these hydroxyl groups can form O-glycosidic bonds with carbohydrate residues to form glycoproteins.
8. Reaction of the amide group: The amide groups of Glutamine and Asparagine can form N glycosidic bonds with carbohydrate residues to form glycoproteins.
9. Reactions of SH group: Cysteine has a sulfhydryl (SH) group and it can form a disulphide (S-S) bond with another cysteine residue. The two cysteine residues can connect two polypeptide chains by the formation of interchain disulphide bonds or links (Fig. 4). The dimer formed by two cysteine residues is sometimes called Cystine or Dicysteine.
Fig4. Formation of disulphide bridge
 الاكثر قراءة في الكيمياء الحيوية
الاكثر قراءة في الكيمياء الحيوية
 اخر الاخبار
اخر الاخبار
اخبار العتبة العباسية المقدسة

الآخبار الصحية















 "المهمة".. إصدار قصصي يوثّق القصص الفائزة في مسابقة فتوى الدفاع المقدسة للقصة القصيرة
"المهمة".. إصدار قصصي يوثّق القصص الفائزة في مسابقة فتوى الدفاع المقدسة للقصة القصيرة (نوافذ).. إصدار أدبي يوثق القصص الفائزة في مسابقة الإمام العسكري (عليه السلام)
(نوافذ).. إصدار أدبي يوثق القصص الفائزة في مسابقة الإمام العسكري (عليه السلام) قسم الشؤون الفكرية يصدر مجموعة قصصية بعنوان (قلوب بلا مأوى)
قسم الشؤون الفكرية يصدر مجموعة قصصية بعنوان (قلوب بلا مأوى)